常常说“秃如其来”,但导致秃头的真正原因你知道吗?
11月17日,鹅厂发布了一项利好每个互联网从业者打工人的重要AI医学进展——秃头元凶“SRD5A2”的蛋白质结构被首次破解了!
来自腾讯AI Lab的医疗AI专家,采用“从头折叠”的蛋白质结构预测方法,帮助解析了原子级别的SRD5A2高分辨率晶体结构,并通过自研AI工具“ tFold”,进一步提升了蛋白质结构预测精度——这意味着,此前一直“黑盒式”存在的脱发关键因子“II型5a还原酶(SRD5A2)”的三维结构终于被首次打开。

更振奋人心的是,治脱药物“非那雄胺”的防脱机制,也被精确鉴定。
长远来看,科学家们根据SRD5A2的蛋白质结构,研发一款更加对症下药、药到病除的防脱新药,已经指日可待了~
这项研究成果,还得到了Nature子刊的官方盖章认可,相关论文日前已经于《 Nature Communications》发表,由南科大生物系魏志毅副教授课题组与匹兹堡大学张诚教授、新加坡 A*STAR 研究所范昊研究员、腾讯 AI Lab 黄俊洲博士带领的研究小组合作完成。

这次新发现,不仅可以用于治疗脱发,其他蛋白质分子和病理学机制的研究也都能用上,具有重要价值。
- 激素变化是导致脱发最主要的原因之一
二氢睾酮是人体中已知最强的雄激素,水平过高的二氢睾酮会带来前列腺增生和脱发等等一系列困扰。
而二氢睾酮正是由前面介绍过的 SRD5A2 催化合成。
所以,当患者因为二氢睾酮水平过高而出现前列腺增生和脱发问题时,目前比较常用的治疗方式,是通过抑制 SRD5A2 来降低患者二氢睾酮水平。
作为 SRD5A2 的高效抑制剂,非那雄胺(finasteride)被广泛用于治疗这类疾病。
虽然 SRD5A2 如此重要和关键,它的高分辨率结构信息却一直是个“黑盒”
最主要的技术难点, 是SRD5A2 具有独特的七次跨膜结构,其与人类全部已知结构的蛋白在结构上差异很大,难以通过现在比较常用的“模板建模”方法获得初始构型来解析晶体数据。
而腾讯 AI Lab 自研的AI工具“tFold”成为破解 SRD5A2 蛋白这一重要难题的关键。
鹅厂技术专家采用了相比“模板建模”难度更高的“从头折叠”方法, 可以不依赖于模板来预测蛋白结构。
在 tFold 工具上进行的三项技术创新,则大幅提升了“从头折叠”方法蛋白结构预测的精度:
首先,实验室研发了“多数据来源融合”(multi-source fusion)技术,来挖掘多组多序列联配(multiplesequence alignment, MSA)中的共进化信息。
然后,借助 “深度交叉注意力残差网络” (deep cross-attention residual network,DCARN),能极大提高一些重要的蛋白2D结构信息(如:残基对距离与取向矩阵)的预测精度。
最后,通过一种新颖的“模板辅助自由建模“(Template-basedFree Modeling, TBFM)方法,将自由建模(Free Modeling, FM)和模板建模(Template-based Modeling, TBM)生成的3D模型中的结构信息加以有效融合,从而大大提高了最终3D建模的准确性。
在腾讯 tFold 工具加持下得到的从头折叠的结构模型,能通过分子置换将 SRD5A2 的结构确定为2.8Å 原子级别高精度。
这一结果能直接推进我们对体内 SRD5A2 活性失调引发的各类疾病的理解,进而为基于 SRD5A2 结构的药物开发提供更多有价值的参考信息。
- tFold 平台的价值也已被学界和业界所看到
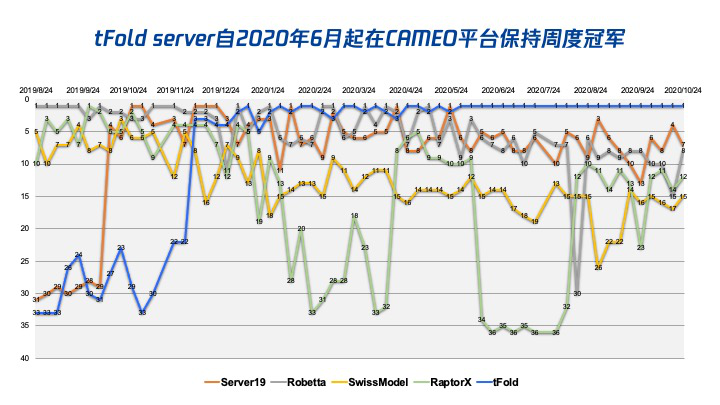
在研究方面,tFold 平台已在国际公认最权威的测试平台 CAMEO 上证明了它的创新价值及有效性。
腾讯 AI Lab 于2020年初在 CAMEO 平台注册了自动化蛋白结构预测服务器 tFold server,并自2020年6月起至今一直保持周度、月度、季度、半年度冠军。tFold server 在一般案例上领先业内权威方法6%以上,在困难案例上则领先12%以上。
在应用方面,tFold server 的公测版也已经在腾讯「云深智药」平台发布。

用户可以手动输入待预测的氨基酸序列或从本地上传 FASTA 格式的序列文件。在经过一定时间的计算之后,用户即可得到使用“从头折叠”方法预测得到高精确度蛋白结构。
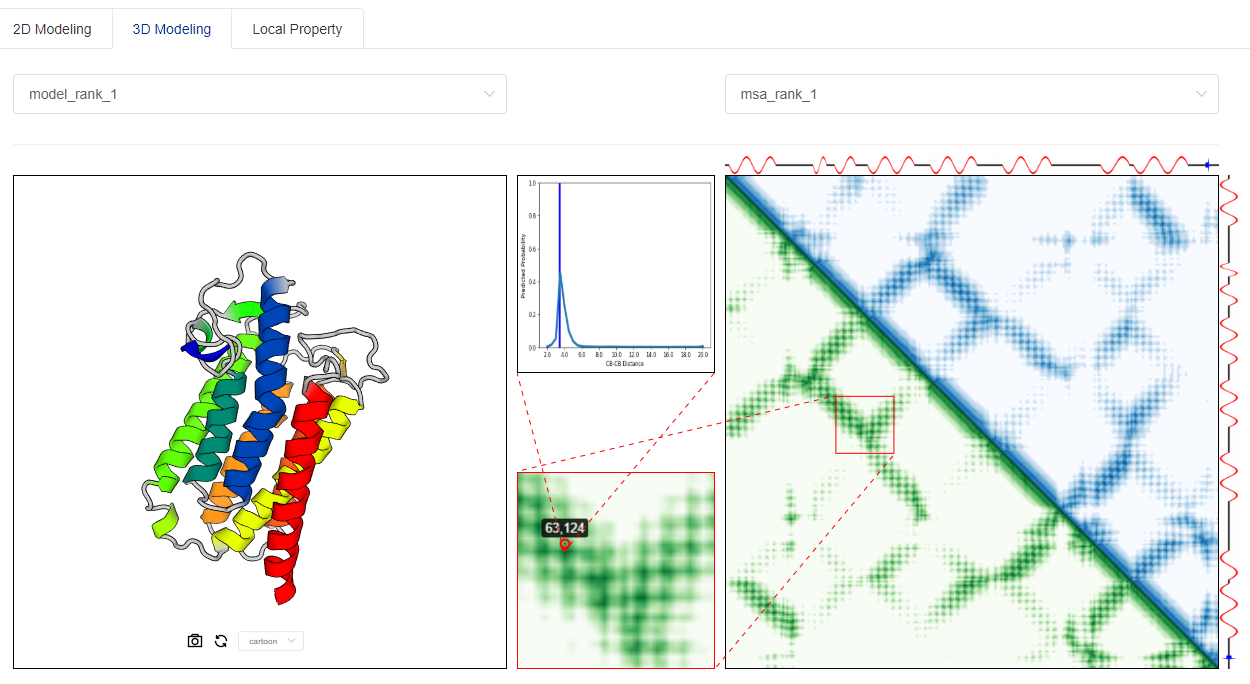
tFold server的3D Modeling输出页面。左边部分为从头折叠得到的3D蛋白模型;右边部分是该3D模型在给定2D距离矩阵下的偏差。
依托大数据挖掘与机器学习等先进技术优势,鹅厂的技术人们正致力于推动AI与医疗产业的深度结合,为社会整体医疗水平提升提供助力~
真诚祝愿未来有一天,世界和平,没有秃顶!
-END-